| Autore |
Discussione |
|
|
sofficemio
Nuovo Arrivato

18 Messaggi |
 Inserito il - 05 febbraio 2009 : 23:11:10 Inserito il - 05 febbraio 2009 : 23:11:10




|
|
chi sa dirmi come si dispongono in ordine crescente di aciditŕ ,basicita e stabilita dei composti.secondo quali regole mica si possono imparare tutte le aciditŕ ecc.
|
|
|
|
|
zerhos
Utente Junior


Prov.: Pisa
Cittŕ: Pisa

421 Messaggi |
 Inserito il - 06 febbraio 2009 : 05:33:32 Inserito il - 06 febbraio 2009 : 05:33:32





|
il concetto di acido-bese č sempre relativo,nel senso che non esiste una scala di valutazione assoluta,ma dipende dai composti che analizzi di volta in volta,per cui se su due composti uno si deprotona piů dell'altro,fungerŕ da acido e l'altro da base.
cmq ci sn delle indicazioni:
per definizione tutti gli acidi organici sono acidi deboli(sempre in relazione agli acidi inorganici che sn piů forti)
in genere si puň dire che tanto piů una molecola č stabile e tanto piů facilemtne tende a deprotonarsi e quindi tanto piů č acida,viceversa per le basi,ad esempio i fenomeni di delocalizzazione rendono la molecola piů stabile perchč disperdono la carica negativa rimanente dopo la deprotonazione,ecco perchč ad esempio gli acidi(con gruppo funzionale cooh per intenderci) sono piů acidi degli alcoli! |
"l'unica differenza tra me e un pazzo č che io non sono pazzo!"
Salvador.Dalě
|
 |
|
|
klodin
Nuovo Arrivato

23 Messaggi |
 Inserito il - 04 aprile 2010 : 12:21:37 Inserito il - 04 aprile 2010 : 12:21:37




|
| help !!!! help!!! c'č qualcuno di buona volontŕ che sa aiutarmi cn alcune scale di aciditŕ e confronti di basicitŕ? |
 |
|
|
lachimica
Utente Junior


Prov.: Pisa

346 Messaggi |
 Inserito il - 06 aprile 2010 : 11:27:48 Inserito il - 06 aprile 2010 : 11:27:48





|
per l'aciditŕ:
devi valutare
1) la differenza di elettronegativitŕ tra gi atomi che formano il legame che deve ionizzarsi:
es
O-H si ionizza meglio di C-H
2) la stabilitŕ della base coniugata che i forma:
es
R-SO3H <- -> H+ + R-SO3- = ibrido di 3 strutture di risonanza equivalenti
R-COOH <- -> H+ + R-COO- = ibrido di 2 strutture di risonanza equivalenti
=> R-SO3H č piů acido di R-COOH
per la basicitŕ
devi valutare
1) quanto č disponibile il doppietto elettronico sul sito basico per essere donato ad H+
es.
piridina č meno basica delle ammine alifatiche perchč N č ibridizzato sp2 invece che sp3 e quindi ha una maggiore % di carattere s ed č piů elettronegativo
anilina č meno basica delle ammine alifatiche perchč il dopietto su N č in parte delocalizzato sull'anello aromatico
2) la stailitŕ dell'acido coniugato che si forma
es. la guanidina č la piů forte base organica: il suo acido coniugato č un ibrido di 3 strurtture limite di risonanza equivalenti! |
 |
|
|
AmOeNuS
Nuovo Arrivato


19 Messaggi |
 Inserito il - 13 luglio 2011 : 19:03:24 Inserito il - 13 luglio 2011 : 19:03:24




|
Sto impazzendo!
Nel fare una scala di basicitŕ ho ottenuto l'acido coniugato dei composti in questione. Fino qui nessun problema! Ma, nel momento in cui vado a scrivere le varie strutture di risonanza, mi blocco.
Ad esempio, partiamo con un composto semplice: lo ione anilinio (che č l'acido coniugato della anilina); bene qui non riesco a spostare nessun doppietto elettronico che mi permetta di delocaliccare la carica positiva!
Immagine:
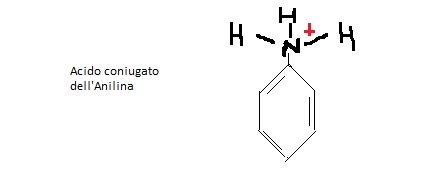
9,98 KB
Come faccio a far muovere quella maledetta carica positiva?
E allo stesso modo:
Immagine:
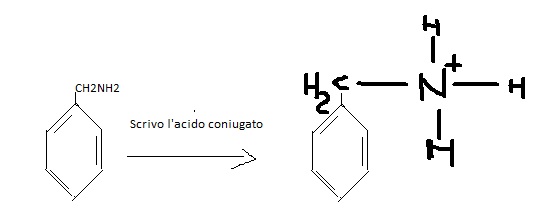
15,73 KB
spero che qualcuno abbia la pasienza di rispondermi, ve ne sarei molto grato. |
 |
|
| |
Discussione |
|






