Malattie genetiche e Progetto Genoma Umano
L11 maggio 2004 sono stato invitato a relazionare in un ciclo di conferenze organizzate dal Circolo Culturale Galileo di Trepuzzi intitolate Invito alla conversazione. 1° edizione della manifestazione, il ciclo di conferenze si è protratto dal 20 aprile fino al 1 giugno. Gli argomenti delle conferenze sono state in gran parte dedicate alla medicina e alla biologia.
Si è parlato di Chiropratica, infarto miocardio, malattie psicosomatiche, naturopatia; a me è stato chiesto di parlare di un tema che ho molto a cuore: Malattie genetiche e Progetto genoma Umano.
La notizia mi ha fatto sorridere poiché essendo laureando in Scienze Biologiche Agroalimentari con tesi sperimentale in genetica di popolazioni, non può che essere un onore preparare una conferenza su questo tema.
Prima che iniziassero tutte le conferenze mi fù consegnato il programma degli incontri ed i temi che questi riguardavano. Tutti i relatori oltre che laureati già da tempo, erano professionisti in materia, lavorano tuttora in ospedali o in centri di ricerca.
Io ero un laureando con pochi titoli in tasca, ed effettivamente pensavo che lintenzione di relazionare di fronte a queste persone potesse essere troppo ambiziosa.
Per prepararmi meglio ho seguito tutte le conferenze e devo dire che la presenza in pubblico non è stata eccezionale, in poche parole la sala non è stata mai piena completamente.
Dopo alcuni mesi è arrivato il mio turno, mi aspettavo poca gente poiché da un laureando cosa mai ci si può aspettare? E invece la sala era piena zeppa di persone, e molte di queste erano i relatori delle altre conferenze.
La mia preoccupazione in quel momento non è diminuita poiché mi chiedevo e se dopo mi vanno a fare domande che non so? beh devo dire che questo aspetto è andato a mio favore però lo lascio alla fine della relazione.
Per uno studente di branche agroalimentari può risultare difficile parlare di genetica medica, ma le tecnologie ricombinati stanno interessando i vegetali come vettori o produttori di nuovi farmaci, penso che ormai la biologia molecolare del Dna debba avere orizzonti aperti per trarre il miglior beneficio possibile.
Quando si parla di malattie genetiche si cita il Dna, i cromosomi e quindi le cellule; proprio con la struttura della cellula ho cominciato la mia conferenza indicando le varie funzioni del nucleo, del reticolo endoplasmatico, dellapparato del Golgi e ho paragonato la cellula ad una fabbrica di automobili poiché la fabbrica di automobili è suddivisa in alcuni comparti specifici per la costruzione di ogni pezzo: in un comparto viene fabbricato il carburatore, in un altro il motore, ecc. Lo scopo di tutto ciò è costruire un automobile; beh il funzionamento della cellula è analogo poiché essa è suddivisa in comparti che funzionano per una specifica funzione. Lo scopo è quello di avere una proteina processata formata da amminoacidi avuti dalla traduzione dei codoni dellRNA messaggero.
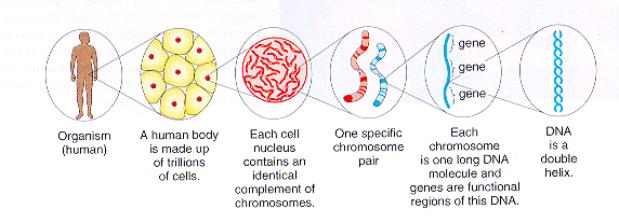
Quando mRNA viene tradotto sui ribosomi basta un singolo errore a livello di una sola base azotata per provocare gravi patologie. Per fare un esempio banale quando lemoglobina deve formarsi, per avere lesatta struttura proteica serve un codone GAG. Da questa tripletta viene tradotto acido glutammico, utile per lesatta conformazione. Se a posto di GAG abbiamo GUG viene tradotta valina. Questa non funziona bene come lacido glutammico e lega le due catene proteiche male provocando la patologia Anemia Falciforme. È solo un piccolo esempio di quello che sono le malattie genetiche.
In questo elaborato parlerò di malattie genetiche, del lavoro del genetista e di quanto sia stato importante nel mondo il progetto genoma umano per unificare le forze e i lavori dei singoli ricercatori.
Il lavoro del genetista. Il lavoro del genetista a mio parere è uno dei più entusiasmanti poiché ci si trova a dover studiare in diretta il comportamento dei geni. Sicuramente il biologo molecolare è più addetto alla biochimica o allo studio molecolare del Dna.
Il genetista può divenire quindi un consulente medico che insieme ad altre figure professionali finalizza diagnosi e prognosi della malattia.
Gli obiettivi che egli deve raggiungere sono diversi: egli deve capire le informazioni mediche inclusa la diagnosi, il decorso della malattia e in base a ciò pianificare gli interventi di prevenzione e terapeutici.
Per acquisire i dati come primo approccio, dobbiamo costituire un albero genealogico. E una descrizione grafica delle generazioni della famiglia dove si sono verificati dei casi di malattia. Da questo esperimento ricaviamo se la malattia è autosomica o determinata dal sesso, se dominante o recessiva.
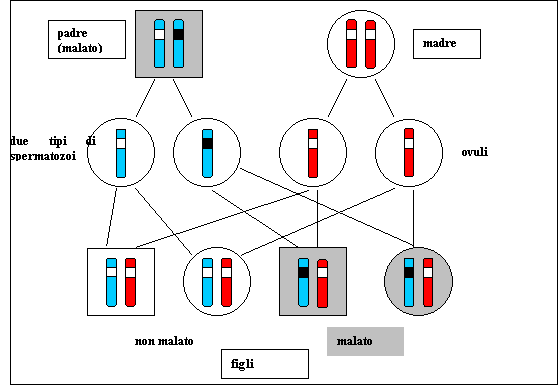
Come primo tipo di patologia osserviamo una trasmissione di malattia Autosomica dominante. In questo grafico possiamo osservare che il padre è un eterozigote malato e la madre è sana. Accoppiandosi questi producono dei tipi di spermi e ovuli che nelle possibili combinazioni vanno a colpire sia maschi che femmine.
 Fonte "British Medical Association Human genetics: Choice and responsibility" , 1998
Fonte "British Medical Association Human genetics: Choice and responsibility" , 1998 Nella eredità autosomica dominante il carattere è presente sempre in proporzioni simili in entrambi i sessi, il carattere è trasmesso alle generazioni successive in entrambi i sessi, ogni persona affetta ha almeno un genitore affetto, circa il 50% dei figli di un genitore affetto sarà affetta, non ci sono salti apparenti di generazione e la malattia è presente in tutte le generazioni.
Un esempio di malattia autosomica dominante è la còrea di Hunghtington, che si manifesta alletà di circa 40 anni con la demenza. E una malattia neuro degenerativa. Il malato prima di arrivare alletà sopradetta pensa di essere sano ma purtoppo il guaio è qui, si accoppia fa dei figli con patologie che si verificheranno di sicuro. Quando la malattia si verifica in tarda o media età viene chiamata a esordio tardivo. Se una malattia era destinata a manifestarsi e non si manifesta si dice che è avvenuto un difetto di penetranza. Il genotipo è malato ma lindividuo è sano. Questo è un caso che avviene quando delle malattie hanno espressività variabile oppure può verificarsi la cosiddetta eterogeneità genetica.
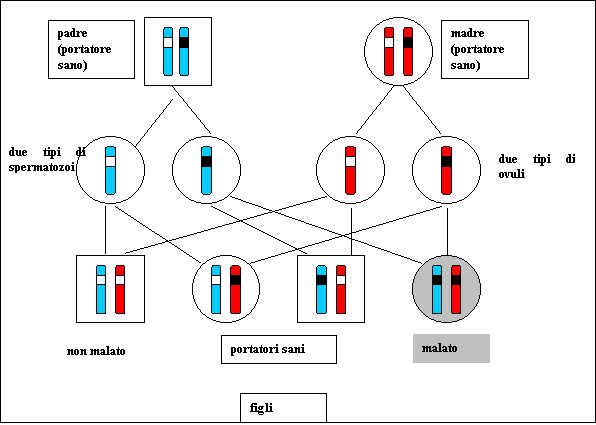
La trasmissione della malattia può avvenire anche in modo Autosomico recessivo.
 Fonte:"British Medical Association Human genetics: Choice and responsibility", 1998
Fonte:"British Medical Association Human genetics: Choice and responsibility", 1998 In questo caso gli individui affetti di solito sono figli di individui non affetti, i genitori degli individui affetti sono , generalmente, eterozigoti asintomatici; entrambi i genitori di un figlio sono portatori della mutazione, la patologia è presente in proporzioni simili ai due sessi, circa il 25% dei figli di portatori sarà affetto, il 50 % dei figli di portatori sarà portatore, il 25 % di figli di portatori sarà sano. La consanguineità aumenta il rischio.
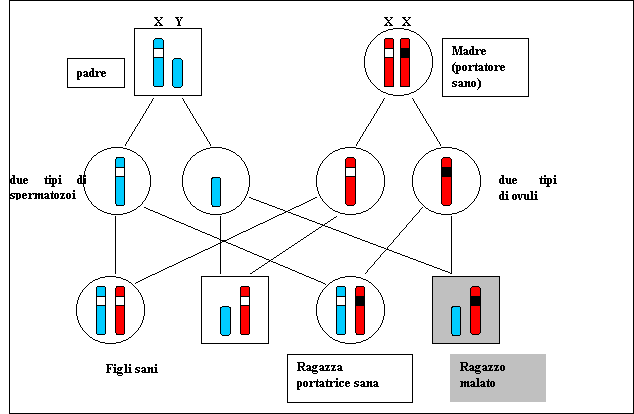
Ora andiamo ad osservare tutte le patologie associate al sesso.
 Fonte:"British Medical Association Human genetics: Choice and responsibility", 1998
Fonte:"British Medical Association Human genetics: Choice and responsibility", 1998 Questo tipo di trasmissione è recessiva associata al cromosoma X colpisce quasi esclusivamente i maschi, quelli affetti nascono da madri eterozigoti e asintomatiche, in media il 50 % dei figli maschi di una madre eterozigote risulterà affetto, si verifica unassenza di trasmissione da maschio a maschio, tutte le figlie di un padre affetto saranno portatrici dette obbligate, i maschi normali non trasmettono la mutazione. Un esempio è la distrofia muscolare di Duchenne.
Una patologia può essere anche causata da una eredità dominante associata al cromosoma X dove le femmine sono circa il doppio rispetto ai maschi, un maschio affetto genera tutte le femmine affette e tutti i figli maschi sani, spesso le femmine sono affette in modo più lieve rispetto ai maschi, data la presenza del cromosoma X normale. Un esempio clinico di questa eredità è il rachitismo iposfatemico.
Oppure può avvenire una eredità legata al cromosoma Y dove colpisce solo i maschi e tutti i figli di un padre affetto sono affetti.
Dopo che si è costituito un albero genealogico si devono acquisire i dati clinici riguardanti tutta la famiglia, questi dati sono definiti anamnestici. Con alberi genealogici e dati anamnestici si può fare una valutazione clinica.
I test che riguardano lo stato clinico del paziente possono essere diversi: test diagnostici, di identificazione dei portatori sani, preclinici e presintomatici, di suscettibilità, per lo studio della variabilità individuale, farmacogenetici. Si possono anche fare delle diagnosi prenatali come amniocentesi, villocentesi e cordocentesi.
Le patologie studiate. - LEUCEMIA MIELOIDE CRONICA
E una malattia molto grave che colpisce il sistema di costituzione del tessuto sanguigno poiché gli ammalati non riescono ad avere cellule del sangue differenziate a sufficienza per proseguire una vita normale.
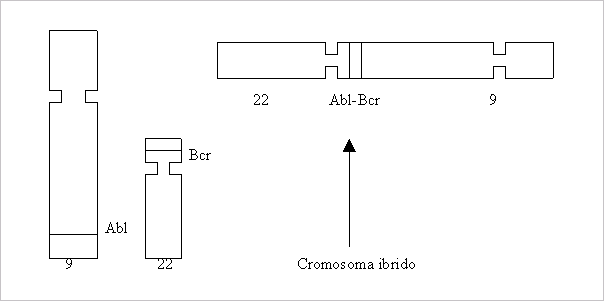
La causa primaria sta a livello del Dna, in particolare per una traslocazione che avviene a livello dei cromosomi 9 e 22, chiamati Philadelfia (paese dove sono state studiati).
Il cromosoma 9 è molto più consistente del 22, ospita il gene Abl mentre il 22 presenta in una banda del braccio lungo il gene Bcr. Entrambi allo stato mutato provocano la leucemia poiché codificano per le proteine Tirosina Chinasi cioè enzimi che fosforilano i substrati a livello dei residui di tirosina, ma che non posseggono funzioni recettoriali a livello di membrana plamatica.
Il gene Abl è capace quindi di attivare le proteine RAS che determinano la cascata di altre proteine TK che a loro volta portano al via di meccanismi di proliferazione cellulare.
Succede in alcuni casi durante la costituzione dei cromosomi, durante la spermatogenesi che avvenga una traslocazione del cromosoma 22 in coda al 9 in modo che il gene Abl e Bcr si fondino formando un gene ibrido. Questo codifica per un proteina di 210 Kd che è allorigine del meccanismo di trasformazione leucemica. Questa proteina è causa oltretutto del 50% dei casi di leucemia acuta linfoblastica (LAL).
La fusione tra Abl e Bcr provoca in primo luogo la cascata incostante ed esagerata che porta al potenziale leucemico, si producono tante cellule emopoietiche ma poche di queste si differenziano e cè anche ridotta apoptosi.
Studiata la proteina ibrida si è capito che era necessaria una sostanza inibente mancante che regolasse lazione del gene Abl.
La sostanza viene oggi prodotta tramite tecniche del DNA ricombinante sui batteri e si chiama Imatinib mesilato, è un principio attivo che troviamo in un farmaco chiamato Glivec.
- TALASSEMIA
È una malattia che può avere differenti varianti caratterizzate da un difetto della sintesi di emoglobina. Lemoglobina è formata da un gruppo proteico ed un gruppo prostatico (eme). Quelli proteici possono essere di tipo alfa, gamma e beta e i difetti proprio su questi provocano le talassemie specialemente per ciò che riguarda le forme alfa e beta e si tratta di malattie a trasmissione autosomica recessiva. Delle due la più diffusa è la beta o anemia mediterranea provocata dalla sintesi di valina al posto di acido glutammico che provoca la caratteristica falciforme.
I geni inerenti per questo tipo di sintesi si trovano sul braccio P del cromosoma 11 e sono state identificate 200 mutazioni.
In condizioni di eterozigoti lindividuo è portatore sano, in caso di omozigosi si ha il morbo di Coolei che porta alla formazione di globuli rossi più piccoli e con minore emivita. Sia per la dimensione che per il ridotto numero presentano bassa attività. La milza di conseguenza ne produce in grandi quantità e aumenta di volume (splancnomegalia) per far arrivare gli eritrociti nel midollo osseo.
La terapia che oggi è attuata si basa sulle trasfusioni e farmaci ferrochelanti. I focolai si notano in Sardegna (12-19%) e provincia di Ferrara (10-20%).
- GLAUCOMA
Malattia dellocchio caratterizzata da un aumento della pressione endoculare dovuto ad un ostacolo dello scarico dellumore acqueo che avviene normalmente attraverso la rete trabecolare che è situata nellangolo irido - corneale.
La patologia la possiamo identificare da tre differenti fenotipi: il Cronico Semplice caratterizzato da un rallentamento del drenaggio dellumore acqueo ed è ereditario. I sintomi sono laumento della pressione endoculare, pallore della pupilla. Riduzione del campo visivo, cecità se non curato.
Ad Angolo Chiuso quando il riassorbimento dellumore acqueo è impossibile poiché cè unalterazione delliride cornea. I sintomi si notano con il dolore, fotofobia, nausea, vomito, indurimento del globo oculare, si deve intervenire urgentemente per evitare la cecità.
Il terzo tipo è il Congenito che si manifesta dal I anno di età, sintomi analoghi, si pratica intervento chirurgico.

Cromosoma 1, regione interessante glaucoma.
- FIBROSI CISTICA
E un disturbo delle cellule epiteliali caratterizzato dallinsufficienza pancreatica, sudorazione salina, produzione di muco nei polmoni. Il problema grave si avverte proprio quando il muco a livello degli alveoli è eccessivo, tale da compromettere il processo di respirazione.
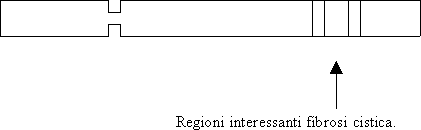
Il gene che codifica è CFTR ed è situato sul cromosoma 7. La proteina risultante è costituita da 1500 amminoacidi. Nella maggior parte dei casi la mutazione consiste nellassenza di uno specifico amminoacido Fenilalanina che si trova a circa un terzo della proteina.
Ci sono tante altre patologie che andrebbero descritte come il morbo di Alzheimer o lHuntington che interessano il sistema nervoso e che si stanno studiando in grande linea. Proprio su questo sito ho letto recentemente notizie che riguardano sia gli studi che le applicazioni pratiche di terapia genica come RNAi per ciò che riguarda la seconda patologia sopra nominata.
Le patologie che ho trattato sono state quelle che ho descritto nella conferenza, qualora il lettore sarà interessato anche a qualsiasi altra patologia potrà richiedermi spiegazioni.
Il progetto genoma umano, quale progetto genoma umano italiano?
Leggendo vari articoli e diversi libri mi sono reso conto di una cosa: il progetto genoma umano è un esempio di come la nostra nazione sia sempre indietro a livello di tempi rispetto alle altre. La scienza italiana per ciò che riguarda la genetica e la biotecnologia deve sempre aspettare gli avventi di altre per poi proseguire. Per fortuna questo accade alla scienza ma gli scienziati sono lavanguardia nel mondo. Potrebbe sembrare una contraddizione ma non lo è, poiché gli scienziati italiani emigrano e lavorano allestero: grave emblema!
Ora io non starò a spiegare i metodi anche perché sono spiegati benissimo nel sito. Voglio interessarmi su principio che grava in Italia: il basso rispetto per la scienza e la scarsa tutela della stessa. Ho già espresso il mio disappunto nel dossier sugli OGM ma cè da aggiungere in questo caso che anche quando lItalia è entrata a lavorare nel progetto si è osservato un certo graduale abbandono poiché i governi esistenti non hanno finanziato e tutelato la ricerca scientifica come a dovere. I fondi oggi arrivano grazie a Telethon e grandi passi avanti si sono fatti per questo.
Invito tutti i lettori a leggere Il progetto genoma umano; un lezione per lItalia del dott. Paolo Vezzoni, ricercatore presso lIstituto di tecnologie Biomediche Avanzate del CNR di Segrate (MI).
BIBLIOGRAFIA
Edoardo Boncinelli- Genoma il grande libro dellUomo.
Giuseppe Novelli, Emiliano Giardina- Genetica medica Pratica.
Paolo Vezzoni- Il progetto genoma umano: una lezione per lItalia.
Inoltre si ringrazia lamica Chiara Papa e tutto il personale dei laboratori dei Genetica e Igiene del dipartimento di Scienze e Tecnologie Biologiche ed Ambientali dellUniversità degli Studi di Lecce, per il sostegno e lincoraggiamento datomi fino adesso.
Inoltra:
 |
Vota: 
|
|
